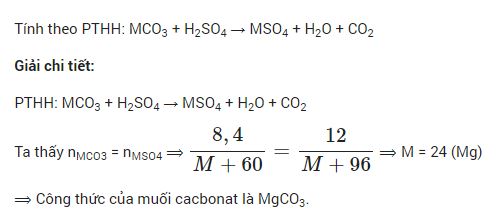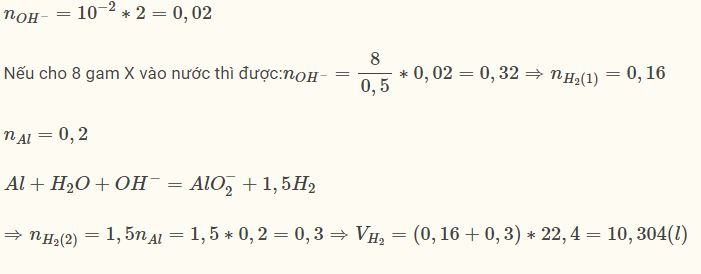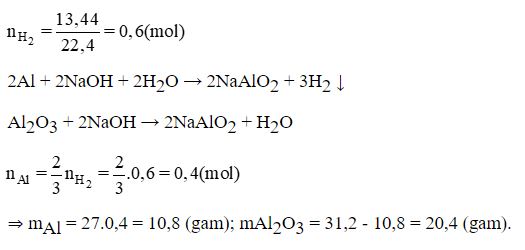Đề thi thử giữa học kỳ 2 môn Hoá Học lớp 12 online - Mã đề 01
Vui lòng cài đặt đề thi trước khi làm bài
Công thức của phèn nhôm – kali
Phản ứng nào sau đây giải thích sự tạo thành thạch nhũ trong hang động
Loại đá và khoáng chất nào sau đây không chứa canxi cacbonat
Cho 200 ml dung dịch AlCl3 1,5M tác dụng với V lít dung dịch NaOH 0,5M, lượng kết tủa thu được là 15,6 gam. Giá trị lớn nhất của V là:
Rb là kim loại thuộc nhóm
Nhỏ từ từ cho đến dư dung dịch NaOH vào dung dịch AlCl3. Hiện tượng xảy ra là
Có bốn chất: Na, Mg, Al, Al2O3. Có thể phân biệt bốn chất trên chỉ bằng một thuốc thử là chất nào sau đây?
Al không tác dụng với dung dịch nào sau đây
X là kim loại nhẹ, màu trắng bạc, rất dẻo, nóng chảy ở nhiệt độ không cao lắm. X là
Trong quá trình điện phân dung dịch KBr, phản ứng nào sau đây xảy ra ở cực dương?
Sục 8,96 lít khí CO2 (đktc) vào dung dịch có chứa 0,25 mol Ca(OH)2. Số gam kết tủa thu được là
Ðun nóng hoàn toàn hỗn hợp CaCO3, Ba(HCO3)2, MgCO3, NaHCO3 đến khối lượng không đổi, thu được sản phẩm chất rắn gồm
Cho 200 ml dung dịch X gồm NaAlO2 0,1M và Ba(OH)2 0,1M tác dụng với V ml dung dịch HCl 2M thu được 0,78 gam kết tủa. Giá trị lớn nhất của V là
Nguyên tắc làm mềm nước cứng là: A. Loại bỏ ion Ca2+ và ion Mg2+ trong nước
Cho dây Pt sạch nhúng vào hợp chất của natri rồi đốt trên ngọn lửa đèn cồn, ngọn lửa có màu
Hoà tan hoàn toàn 8,4 gam muối cacbonat của kim loại M (MCO3)2 bằng dung dịch H2SO4loãng vừa đủ, thu được một chất khí và dung dịch G1. Cô cạn G1, được 12,0 gam muối sunfat trung hoà, khan. Công thức hoá học của muối cacbonat là:
Cho m gam hỗn hợp Na2CO3 và NaHCO3 có số mol bằng nhau tác dụng với dung dịch H2SO4 loãng, dư. Khí sinh ra được dẫn vào dung dịch Ba(OH)2 dư thu được 39,4 gam kết tủa.. Giá trị của m là
Dung dịch Ca(OH)2 tác dụng được với:
Cho phản ứng: aAl + b H2SO4 → c Al2(SO4)3 + d SO2 + eH2O
Hệ số a, b, c, d, e là các số nguyên tối giản. Tổng a + b là
Kim loại phản ứng với nước ở nhiệt độ thường tạo ra dung dịch có môi trường kiềm là
Cho 0,5 gam hỗn hợp X gồm Li, Na, K vào nước được 2 lít dd có pH = 12. Trộn 8 gam hỗn hợp X và 5,4 gam Al rồi cho vào nước đến phản ứng hoàn toàn có V lít khí (đktc). Giá trị của V là
Trong các kim loại sau: Na, Mg, Al, Fe. Kim loại có tính khử mạnh nhất là
Hiện tượng xảy ra khi thả mẩu Na và dung dịch CuSO4
Ion Na+ bị khử khi người ta thực hiện phản ứng:
Cho phản ứng: Al +H2O +NaOH → NaAlO2 +3/2H2
Chất tham gia phản ứng đóng vai trò chất oxi hóa là chất nào?
Cho 31,2 gam hỗn hợp bột Al và Al2O3 tác dụng với dung dịch NaOH dư thoát ra 13,44 lít khí (đktc). Khối lượng mỗi chất trong hỗn hợp đầu là
Chỉ dùng một kim loại hãy phân biệt các dung dịch muối sau NaCl, NH4Cl, FeCl3, (NH4)2CO3, AlCl3
Cấu hình electron lớp ngoài cùng của kim loại kiềm thổ là:
Hòa tan hoàn toàn hợp kim Al - Mg trong dung dịch HCl, thu được 8,96 lít khí H2 (đktc). Nếu cũng cho một lượng hợp kim như trên tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí H2 (đktc). Thành phần phần trăm theo khối lượng của Al trong hợp kim là:
Cho Ba dư tác dụng với dung dịch chứa x mol HCl, thu được a1 mol H2. Cho Fe dư tác dụng với dung dịch chứa x mol HCl, thu được a2 mol H2. Quan hệ giữa a1 và a2 là